CẢNH BÁO VỀ TÁC DỤNG PHỤ CỦA TNF – ALPHA
Ths. BS Phạm Thành Trung (1)
(1) Đơn vị Da liễu & Thẩm mỹ da – Bệnh viện Đại học Y dược Buôn Ma Thuột
Yếu tố ức chế hoại tử bướu alpha (TNF- alpha) là một điều trị quan trọng trong nhiều bệnh viêm bao gồm viêm khớp dạng thấp, vảy nến, hội chứng ruột kích thích. Ức chế TNF – alpha tạo ra một điều trị trúng đích đối lập với điều trị miễn dịch không đặc hiệu thường dùng trong các bệnh viêm. Tuy nhiên, có nhiều tác dụng phụ của ức chế TNF- alpha đã được xác định thông qua các thử nghiệm lâm sàng và các điều tra sau sử dụng.
Những vấn đề này có thể liên quan với các phản ứng tại chỗ chích, suy tim. Một số phản ứng khác của liệu pháp TNF-alpha bao gồm bùng phát lao phổi, nhiễm trùng khác, bệnh ác tính, rối loạn miễn dịch.
1. Đại cương
Tác dụng phụ của ức chế TNF – alpha có thể rất trầm trọng. Tuy nhiên, những nguy cơ này cần được đánh giá trong bối cảnh chung so sánh với lợi ích nhận được và so sánh với tác dụng phụ của các phương pháp điều trị khác cho các bệnh miễn dịch (như là glucocorticoids, methotrexate, cyclophosphamide, azathioprine).
Vì vậy, quyết định có sử dụng liệu pháp ức chế TNF- alpha hay không cần được cân nhắc phù hợp cho từng bệnh nhân dựa vào đặc điểm lâm sàng và các yếu tố nguy cơ riêng lẻ của từng người.
Chất sinh học TNF – alpha
TNF – alpha thường được biết đến là cachexin được mô tả vào năm 1975 và được trình bày khả năng ly giải bướu của trong môi trường invitro và trên chuột thí nghiệm (đây là nguyên nhân của cái tên yếu tố hoại tử bướu). Hoạt động của TNF – alpha chống lại bướu trong phòng thí nghiệm làm tăng khả năng của việc ức chế protein này có thể sẽ làm tăng nguy cơ ác tính. Tuy nhiên các dữ liệu theo dõi lâu dài thì chưa có xác định về vấn đề này.
TNF- alpha hoạt hóa cần ba đơn vị TNF- alpha đơn để tạo thành một cấu trúc bậc ba TNF- alpha, cấu trúc này sau đó sẽ gắn với 1 trong hai thụ thể TNFR1 hoặc TNFR2 (hình 1). TNFR1 và TNFR2 được bến đến là p55 và p75. Cấu trúc bậc ba sau khi gắn với thụ thể sẽ kích hoạt tạo ra cytokines. Cả TNFR1 và TNFR2 đều tạo ra nhiều phản ứng tới hệ miễn dịch bao gồm:
Kích thích tạo ra các cytokines viêm như là Interlerkin -1 beta, IL-6, IL-8 và yếu tố kích thích đại thực bào (GM -CSF).
Kích thích sự bộc lộ và hoạt động của các phân tử nội mạch (ICAM-1, VCAM-1, E-selectin) và các chemokines (MCP-1, MIP-2, RANTES and MIP-1alpha),
Phối hợp cùng với tế bào leukocytes tác động lên cơ quan đích.
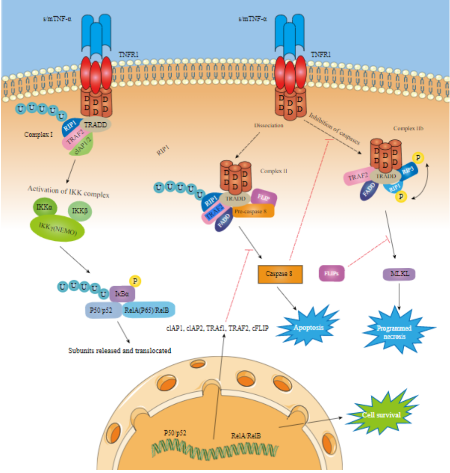
Hình 1: Con đường tín hiệu TNF- alpha
TNF- alpha và cơ chế phản hồi của cơ thể
TNF – alpha quan trọng trong hoạt hóa đại thực bào, hiện tượng thực bào và biệt hóa từ tế bào monocytes thành đại thực bào, triệu tập tế bào đa nhân trung trính và đại thực bào, tạo thành u hạt và duy trì u hạt. Ảnh hưởng của TNF -alpha trên hiện tượng nhiễm trùng đã được thực hiện kiểm tra trên các thí nghiệm động vật bao gồm vật chủ được trung hòa kháng thể, cắt gen biểu hiện TNF- alpha hoặc các thụ thể của nó hoặc là làm dẫn tới sự bộc lộ vượt trội của thụ thể TNF – alpha.
Các thí nghiệm trên động vật đã chứng minh vai trò quan trọng của TNF – alpha trong việc bảo vệ trước nhiều tác nhân bao gồm Mycobacterium tuberculosis, M.avium, M.bovis, Bacillus Calmette- Guerin, Aspergillus fumigatus, Histoplasma capsulatum, Toxoplasma gondii, Cryptococcus neoformans, và Candida albicans.
Đối vận TNF- alpha: Có 5 chất ức chế TNF-alpha đã được thông qua để điều trị các bệnh viêm bởi FDA. Các thuốc này bao gồm:
- Etanercept – Một protein hòa tan kết hợp thụ thể TNF -alpha p75
- Infliximab – Kháng thể kháng TNF – alpha chimeric (kết hợp chuột/ người).
- Adalimumab – Kháng thể kháng TNF – alpha đơn dòng hoàn toàn từ người.
- Certolizumab pegol – Một kháng thể gắn nhánh Fab của kháng thể đơn dòng từ người gắn với polyethylene glycol.
- Golimumab – Kháng thể kháng TNF – alpha đơn dòng hoàn toàn từ người.
Sự khác biệt của các biện pháp: Infliximab và adalimumab đều được chấp thuận cho một phổ lâm sàng rộng hơn là etanercept. Ví dụ, những thuốc trên có thể hiệu quả trong hội chứng ruột kích thích, sarcoidosis cũng như là viêm khớp dạng thấp, viêm khớp vảy nến và nhiều bệnh viêm khác. Mặt khác, etanercepts thì không có hiệu quá trong bệnh IBD hay sarcoidosis.
2.Tác dụng phụ nghiêm trọng
2.1. Phản ứng tại chỗ tiêm
Những phản ứng da đặc trưng bao gồm ngứa, đau, đỏ, kích ứng, sưng phù tại vị trí chích thuốc rất thường gặp, nhưng đều là các vấn đề nhỏ khi tiêm các thuốc dưới da. Những phản ứng tại chỗ chích thường có thể xảy ra trong suốt tháng đầu điều trị và có thể kéo dài ba đến năm ngày. Những phản ứng này có thể điều trị, nếu cần thiết với các phương pháp như là chườm lạnh, bôi corticosteroid tịa chỗ và thay đổi vị trí chích. Việc phải dừng hẳn thuốc chỉ xảy ra ở một số rất ít bệnh nhân.
2.2. Phản ứng quá mẫn
Phản ứng quá mẫn với infliximab có thể chia thành hai dạng:
- Cấp – phản ứng cấp xảy ra trong vòng 24 giờ. Những phản ứng kiểu này thường xảy ra sau 10 phút và trong khoảng 4 giờ sau khi bắt đầu tiêm truyền.
- Trễ – Phản ứng trễ thì có thể xuất hiện trong 1 tới 14 ngày sau khi bắt đầu điều trị, tuy vậy thường gặp là 5 tới 7 ngày.
Cả phản ứng quá mẫn cấp và muộn đều có thể chia thành nhẹ, trung bình và nặng tùy thuộc vào dấu hiệu và triệu chứng. Khoảng hơn 90% các trường hợp quá mẫn do infliximab là quá mẫn sớm.
Phản ứng quá mẫn sớm: Thỉnh thoảng phản ứng quá mẫn sớm thực sự là một phản ứng dịch ứng liên quan IgE (phản ứng dị ứng type 1), phản ứng phản vệ gồm hạn huyết áp, phù khò khè có hay không có mề đay kèm theo.
Phản ứng phản vệ thực sự xảy ra ở một vài bệnh nhân điều trị với infliximab. Tuy nhiên, phần lớn các phản ứng quá mẫn do điều trị với infliximab thường có đặc điểm là không có triệu chứng đặc hiệu và được phân nhóm gần với các phản ứng không phải dị ứng, không liên quan với IgE.
Tần suất và cường độ của phản ứng quá mẫn sớm được thống kê trong một nghiên cứu ở 165 bệnh nhân đã tiêm 479 liều infliximab: có 16 bệnh nhân (10%) có ít nhất 1 lần phản ứng quá mẫn
Phản ứng quá mẫn tự nhiên vẫn chưa rõ cơ chế. Tuy nhiên có hai nghiên cứu đã đưa ra kiến nghị rằng phản ứng quá mẫn sớm không liên quan với phản ứng phản vệ IgE :
- Phản ứng sẽ được giải quyết một cách hiệu quả bằng cách làm giảm lượng thuốc tiêm. Việc tiếp cận này sẽ không hiệu quả với các phản ứng phản vệ.
- Trong một nghiên cứu dưới nhóm ở 11 bệnh nhân đã trải qua tổng cộng 14 lần phản ứng quá mẫn thì tryptase huyết thanh và nồng độ IgE thuyết hanh đều ở mức bình thường trong cả 6 bệnh nhân được đo.
Phản ứng quá mẫn muộn: Phản ứng quá mẫn muộn liên quan với thời gian khởi phát và các đặc điểm: phát ban da, đau khớp, mệt mỏi và thỉnh thoảng có sốt. Phản ứng quá mẫn muộn có thể liên quan tới dị ứng type III.
Một nghiên cứu cắt ngang mô tả được thực hiện tại United states Mediacare cho thấy tần suất phản ứng quá mẫn của bệnh nhân viêm khớp dạng thấp điều trị bằng infliximab, etanercept, rituximab, tocilizumab, golimumab bằng cách truyền hoặc tiêm. Trong khoảng 6 tháng, thì tỷ lệ mới mắc thấm với tỷ lệ mới mắc khoảng 2.4( với abatacept) và 239.5 (rituximab)trên 106 người – ngày.
Phòng ngừa: Nhiều phương pháp phòng ngừa hiệu quả trong phản ứng quá mẫn do infliximab.
- Uống thuốc trước khi truyền: diphenhydramine (25 -50mg) và acetaminophen (650mg) 90 phút trước khi truyền. Hoặc bệnh nhân có thể uống 1 loại kháng histamin thế hai.
- Sử dụng 1 liều thử infliximab. Liều thử sẽ bắt đầu bằng 10ml/giờ, theo sau đó tăng lên mỗi 15phuts cho đến khi đạt liều tiêu chuẩn là 125ml/giờ.
- Với bệnh nhân có tiền sử phản vệ sau sử dụng infliximab, thì việc sử dụng prednisone (50mg mỗi 8 giờ) nên được kê trước 24 giờ trước khi truyền infliximab kèm theo sử dụng diphenhydramine (25 -50mg) và acetaminophen (650mg).
2.3. Giảm tế bào máu
Giảm tế bào đa nhân trung tính có thể xảy ra ở bệnh nhân sử dụng ức chế TNF- alpha, nhưng điều này thường xảy ra nhẹ, những loại giảm tế bào máu khác thì hiếm khi xảy ra. Sự giảm của tế bào đa nhân trung tính thường xảy ra ở những bệnh nhân sử dụng ức chế TNF- alpha. Tuy nhiên, cơ chế của hiện tượng này thì vẫn chưa rõ. Nguy cơ bị giảm tế bào đa nhân trung tính được thẩy rằng cao hơn có ý nghĩa thống kê ở những bệnh nhân có tiền sử bị giảm bạch cầu khi sử dụng các loại thuốc khác.
Hầu hết các bệnh nhân có giảm bạch cầu đa nhân trung tính thì không cần thiết phải ngưng liệu pháp này. Tuy vậy, thì việc giảm kéo dài hay tái diễn cũng thấy ở những người sử dụng các loại ức chế TNF-alpha khác. Vì nguy cơ của giảm bạch cầu đa nhân trung tính ở bệnh nhân sử dụng ức chế TNF-alpha, thì cần thiết phải kiểm tra công thức máu trong vòng 1 tháng khi bắt đầu và lặp lại mỗi ba tới sáu tháng.
2.4. Nhiễm trùng
TNF-alpha là một thành tố quan trọng của hệ miễn dịch đáp ứng với nhiều loại nhiễm trùng. Việc sử dụng ức chế TNF-alpha có thể liên quan với tăng nguy cơ nhiễm trùng nghiêm trọng, đặc biệt là viêm phổi, lao, zona và các nhiễm trùng cơ hội khác.
Tầm soát yếu tố nguy cơ lao phổi cần thực hiện trước khi bắt đầu sử dụng ức chế TNF-alpha bởi vì sự tăng của nguy cơ kích hoạt lao có sẵn.
2.5. Bệnh mất bao myelin
Một liên hệ khả dĩ giữa ức chế TNF-alpha và bệnh mất bao myelin đã được nhắc đến nhưng chưa được chứng minh.
2.6. Suy tim
Ức chế TNF-alpha có thể liên quan với suy tim, tuy nhiên dữ liệu khá đa dạng.
Dữ liệu của việc tăng nguy cơ suy tim với việc sử dụng ức chế TNF- alpha theo liều của FDA chấp thuận thì vẫn chưa được xác định. Tuy nhiên, trên nhãn của etanercept, infliximab, adalimumab luôn kèm khuyến cáo “sử dụng thận trọng với những bệnh nhân bị suy tim hoặc giảm phân suất tống máu thất trái, làm nặng lên suy tim hay khởi phát mới suy tim đã được báo cáo”. Thêm vào nữa, infliximab tập trung với liều cao hơn 5mg/kg ở bệnh nhân có suy tim trung bình hoặc nặng (NYHA III/IV).
Với những bằng chứng hiện nay, thì những bệnh nhân suy tim có triệu chứng, chúng tôi đề xuất rằng lựa chọn điều trị khác sẽ tốt hơn là ức chế TNF-alpha. Ở những bệnh nhân có suy tim tiến triển khi đang điều trị với ức chế TNF-alpha, thuốc cần giảm liều và có thể cân nhắc sử dụng một loại thuốc khác.
Với những bệnh nhân với suy tim phải hoặc suy tim bảo tồn chức năng (NYHA I/II) và viêm khớp không đáp ứng với các thuốc khác, thì điều trị nhắm trúng đích bằng ức chế TNF-alpha có thể cân nhắc.
FDA báo cáo về các trường hợp suy tim:
FDA công bố báo cáo tóm tắt 47 ca suy tim liên quan tới etanercept hoặc infliximab báo cáo tới hệ thống dữ kiện phản ứng phụ nghiêm trọng từ tháng 2 năm 2002. Ba mươi tám bệnh nhân tiến triển suy tim mới và 9 người bùng phát lại suy tim.
Trong 38 người tiến triển suy tim mới thì có 19 người không có yếu tố nguy cơ nào như bệnh mạch vành, tăng huyết áp, tiền sử viêm cơ tim, hay đái tháo đường, 10 người dưới 50 tuổi. Sau khi ngưng ức chế TNF -alpha và bắt đầu điều trị suy tim thì 3 trong số 10 người đã hoàn toàn hồi phục, 6 người tiến triển và 1 người chết.
2.7. Bệnh phổi
Ức chế TNF được sử dụng trong điều trị nhiều bệnh phổi và các bệnh viêm khớp hệ thống có hay không có ảnh hưởng phổi. Các tác dụng phụ lên phổi nghiêm trọng bao gồm:
- Bệnh u hạt : có nhiều báo cáo về bệnh tương sự sarcoid, việc ngưng ức chế TNF- alpha có hoặc không có sử dụng glucocorticoid thường dẫn tới việc giảm triệu chứng.
- Xơ phổi: Hầu hết bệnh nhân bị viêm khớp dạng thấp thì có nhiều bệnh nền liên quan đến phổi và methotrexate thường được sử dụng ở nhóm bệnh nhân này.
2.8. Nhiễm độc gan
Nguy cơ nhiễm độc gan liên quan với ức chế TNF- alpha thì khá nhỏ. Vào tháng 1 năm 2004, có ít nhất 35 báo cáo về những phản ứng nặng tại gan đã được báo cáo tới FDA, dẫn tới cảnh báo một cách nghiêm túc về vấn đề này. Nhiều loại ảnh hưởng gan đã được chú ý tới, bao gồm suy gan, viêm gan, nhiễm mỡ. Bệnh gan hoại tử và những trường hợp phải cần đến ghép gan đã được báo cáo. Cơ chế ảnh hưởng của thuốc làm tổn thương gan, làm gan nhiễm mỡ và bệnh gan miễn dịch.
Nhiều báo cáo của bệnh gan liên quan tới infliximab, thường dùng trong liều cao của bệnh Crohn. Một nghiên cứu lớn thực hiện trên 6861 trường hợp viêm khớp dạng thấp điều trị với ức chế TNF- alpha, cho thấy nồng độ ALT và AST cao hơn 1 lần giới hạn trên của 17.6% số bệnh nhân, và cao hơn 2 lần ở 2.1 bệnh nhân. Nồng độ tăng cao gấp 3 lần, 5 lần được tìm thấy ở 0.57% và 0.13%. Chức năng gan bất thường tăng lên ở những người đồng thời sử dụng methotrexate và leflunomide. Infliximab thì thường thấy hơn là adalimumab, và etanercept thì có vẻ là không có tăng.
Soi sánh với viêm khớp dạng thấp thì các thể viêm khớp khác như viêm khớp vảy nến có liên quan với tỷ lệ đồng mắc bệnh gan cao hơn và có tỷ lệ bệnh gan tự miễn liên quan ức chế TNF- alpha cao hơn. Một báo cáo từ Hàn Quốc thấy rằng có 23.7% bệnh nhân (86 trong số 363) điều trị bằng ứng chế TNF-alpha cho thấy chức năng gan bất thường.
2.9. Các phản ứng trên da niêm:
Có nhiều tình trạng da liễu được báo cáo liên quan với ức chế TNF-alpha. Bao gồm:
- Phản ứng quá mẫn và phản ứng tại nơi tiêm
- Nhiễm virus da niêm (herpes zoster, varicella), nhiễm trùng, nhiễm nấm.
- Thay đổi trong sang thương da vảy nến
- Viêm da cơ địa
- Lupus ban đỏ hiệ thống
- Lichen phẳng
- Hiếm có là rụng tóc.
Sang thương da liên quan với liệu pháp ức chế TNF- alpha được mô tả ở nhiều nghiên cứu với bệnh nhân bị hội chứng ruột kích thích. Sang thương da đặc hiệu gồm chàm dạng vảy nến, chàm, mụn mủ, vảy nến, những bất thường khác có thể gặp bao gồm viêm nang lông vi khuẩn, mụn trứng cá, rụng tóc từng vùng và nhiều dạng viêm da nhiễm trùng khác. Việc điều trị hiệu quả bởi bác sĩ da liễu có kinh nghiệm sẽ xem xét việc tiếp tục hay không tiếp tục liệu pháp ức chế TNF.
3.Tổng kết
Thuốc ức chế yếu tố hoại tử bướu alpha có nhiều nguy cơ phản ứng phụ bao gồm:
- Phản ứng tại nơi chích
- Phản ứng quá mẫn
- Giảm bạch cầu đa nhân trung tính
- Nhiễm trùng
- Bệnh mất myelin
- Suy tim
- Bệnh phổi
- Nhiễm độc gan
- Phản ứng trên da
- Bệnh ác tính
- Bệnh tự miễn
Phản ứng quá mẫn bởi infliximab được chia làm 2 thể:
- Sớm: phản ứng sớm xảy ra trong vòng 24 giờ.
- Muộn: có thể xảy ra trong vòng 1 tới 14 ngày.
Ức chế TNF-alpha có thể liên quan với sự xuất hiện cũng như việc bùng phát suy tim. Bệnh nhân có triệu chứng suy tim thì cần cân nhắc điều trị khác hơn là dùng ức chế TNF-alpha. Ở những bệnh nhân tiến triển suy tim khi đang sử dụng thì cần giảm liều và việc ngừng thuốc cần được cân nhắc.
TÀI LIỆU THAM KHẢO
- García-Doval I, Hernández MV, Vanaclocha F, et al. Should tumour necrosis factor antagonist safety information be applied from patients with rheumatoid arthritis to psoriasis? Rates of serious adverse events in the prospective rheumatoid arthritis BIOBADASER and psoriasis BIOBADADERM cohorts. Br J Dermatol 2017; 176:643.
- Carswell EA, Old LJ, Kassel RL, et al. An endotoxin-induced serum factor that causes necrosis of tumors. Proc Natl Acad Sci U S A 1975; 72:3666.
- Beutler B, Cerami A. The biology of cachectin/TNF–a primary mediator of the host response. Annu Rev Immunol 1989; 7:625.
- Feldmann M, Maini RN. Anti-TNF alpha therapy of rheumatoid arthritis: what have we learned? Annu Rev Immunol 2001; 19:163.
- Zhang G. Tumor necrosis factor family ligand-receptor binding. Curr Opin Struct Biol 2004; 14:154.
- Roach DR, Bean AG, Demangel C, et al. TNF regulates chemokine induction essential for cell recruitment, granuloma formation, and clearance of mycobacterial infection. J Immunol 2002; 168:4620.